“火星登陆计划” 是由复宏汉霖发起的创新招贤榜,旨在集结并携手一群优秀的科学家,以解决未满足的临床需求为目标,直击新药研发、临床诊疗、生物医学研究领域最具潜力和突破可能性的焦点,汇聚产学研角度的智慧,共同破解生物医药领域挑战,探讨并落地最优秀的Idea。
基于细胞的治疗技术是指利用细胞(如免疫细胞、干细胞等)作为活体制剂来治疗疾病的技术。2017年,随着两款靶向CD19的CAR-T药物先后被美国FDA批准上市,tisagenlecleucel用于治疗急性淋巴细胞白血病(ALL)和axicabtagene ciloleucel用于治疗大B细胞淋巴瘤(LBCL),过继性细胞疗法在医药市场上获得了爆发性的关注,越来越多的企业加入了细胞治疗的研发队伍中。除了血液瘤之外,近期细胞疗法也在其它适应症上获批,例如使用自体衍生的角膜干细胞修复受损的角膜上皮细胞[1]、利用干细胞治疗克罗恩病相关瘘管[2]等。
当前细胞治疗的难点和尝试
细胞治疗突破了传统的药物治疗方式,给以往难以治疗的疾病带来了希望,但以CAR-T为代表的第一代细胞治疗技术仍有很多问题有待突破。例如安全性问题,脱靶毒性可能使正常细胞受到误伤,而输入患者体内的细胞也可能不受控地迁移至非病灶部位并在该处增殖,带来潜在的致瘤风险;例如生产制备问题,提取患者自体细胞进行工程改造后再回输至患者体内的过程相对复杂,无法批量化生产,成本高昂,而使用非自体细胞(同种异体细胞)制备现货型细胞产品也需解决质量控制、药效持久性、免疫排斥等问题[3]。
为解决这些问题,并在实体瘤中实现突破,许多公司都在尝试各种改良型和创新型细胞治疗技术。肿瘤浸润淋巴细胞疗法(TIL)是基于T细胞的过继性细胞疗法,其过程无需对T细胞进行工程改造。一些公司已开展临床研究,从患者体内获取肿瘤组织,分离出TIL并在体外使用IL-2细胞因子刺激TIL的扩增,旨在增加TIL的数量、激活TIL的抗肿瘤能力,使得回输的TIL存活更长时间,更有效地杀伤肿瘤细胞。一些公司研发的Tmod T细胞技术通过为T细胞装备双模块——识别肿瘤相关抗原的激活模块,和识别正常细胞抗原的阻断模块,来保护正常细胞免受攻击。此外,γδTCR-T、CAR-Macrophage、CAR-NK等疗法也纷纷进入临床阶段。
诱导多功能干细胞(iPSC)来源的细胞疗法具有可批量化生产通用型细胞的优势,可降低成本、提前制备、随取随用,不少公司已着眼于该疗法的开发,例如将iPSC NK细胞疗法单用或与NK Engager协同,靶向杀伤肿瘤细胞,而IL-15信号的加入可促进NK细胞增殖、提高抗肿瘤活性[4]。另外,iPSC在眼病、神经系统疾病、代谢类疾病等非肿瘤疾病中的应用也在研究中,例如用iPSC来源的视网膜色素上皮细胞治疗急性黄斑变性[5],用iPSC生成多巴胺能神经元治疗帕金森[6],利用iPSC开发替代胰岛B细胞的工程细胞以治疗1型糖尿病[7]等。
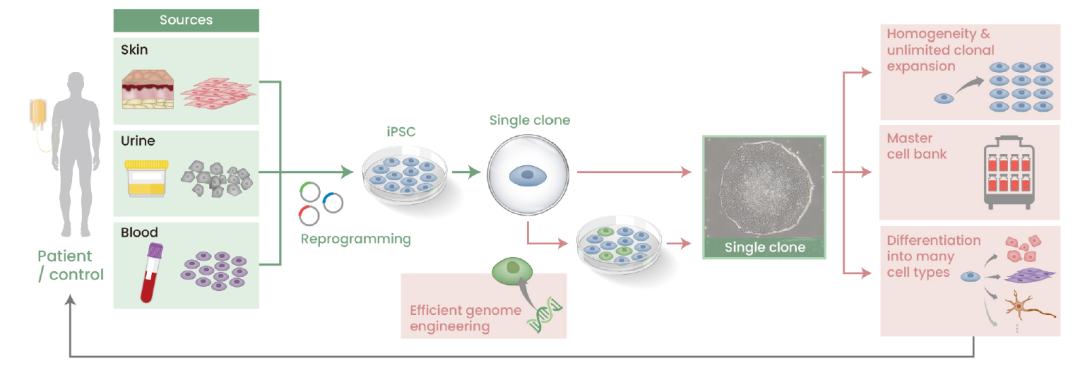
Application of iPSCs to regenerative medicine [4].
创新细胞工程技术助力细胞治疗
基因编辑和表观基因组编辑、合成生物学、生物材料等领域的发展,可助力细胞治疗应对当前的挑战,改善现有疗法,或创建新的细胞治疗管线。除少部分技术已成功用于商业化产品,目前大多数研究仍处于临床前阶段。
CRISPR-Cas基因编辑系统在特定位点制造DNA双链断裂(DSBs),经过细胞自发的修复机制(如NHEJ,HDR等),可对单个位点甚至多个位点实现基因编辑。在一项研究中,科学家使用慢病毒递送Cas9 mRNA和gRNA,同时敲除T细胞受体(TCR)、β2-微球蛋白(β2m)和PD1基因,可制造缺乏TCR、HLA I分子和PD1的同种异体通用型CAR-T细胞,这种经过基因编辑的CAR-T细胞免疫原性降低、生存能力提高,且PD1基因的敲除使其具有更强的抗肿瘤活性,可增加临床使用时的安全性和有效性[8]。
合成生物学通过应用定量设计规则,可使基因工程更加精确、可预测和可重复,例如精确控制治疗性转基因的表达、细胞分泌的治疗因子的传递,或对细胞进行编程后,使其具有特殊的感知和反应能力,感知组织相关或疾病状态相关的分子并改变细胞行为,这些改造可增强细胞治疗的效果。
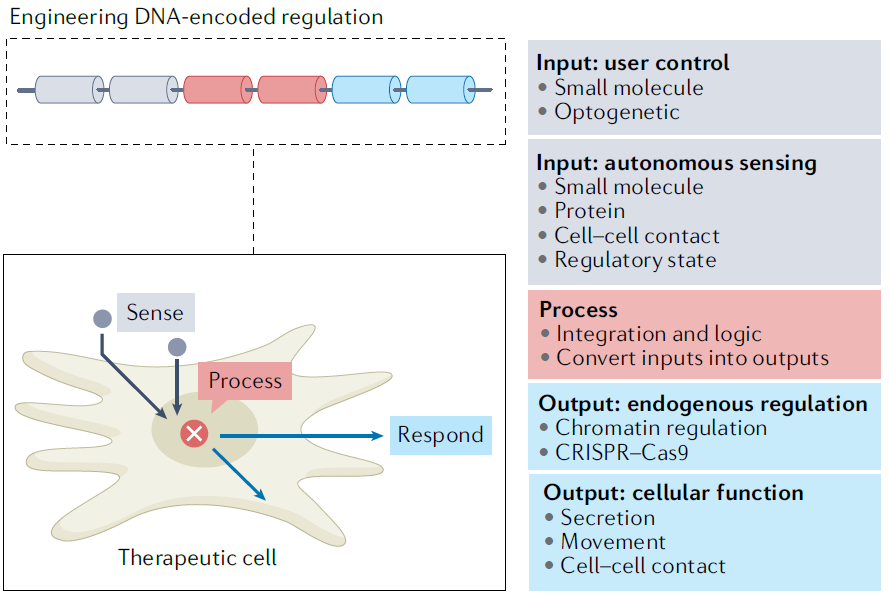
Using synthetic biology approaches to endow therapeutic cells with enhanced functional properties[3]
生物材料的使用(半渗透性生物材料、水凝胶等)可辅助治疗用细胞的递送,保证其生物活性和安全性。当前研究的重点在于开发长效的功能性免疫分离技术,保护治疗用细胞免受人体免疫细胞的排异,以实现异体细胞的使用。对异体细胞排异反应的产生需经过细胞间的接触,因此用半渗透性材料将治疗用异体细胞进行封装是一种应对策略,这种封装需考虑异体细胞与外界的双向物质交换,例如从外界流入葡萄糖、氧气等养分以维持细胞生命,从内部流出工程细胞产生的治疗性蛋白分子。生物材料细胞封装技术已在肿瘤、内分泌、神经内分泌、眼科疾病等领域开展临床评估,但其中一个挑战在于,免疫细胞对这些生物材料的排异反应会使材料内部逐渐产生纤维化和缺氧问题,难以实现长期有效的治疗效果。面对该挑战,科学家正在尝试使用海藻酸基水凝胶、ultra-low-fouling两性离子生物材料等新型材料,并在动物实验中观察到了积极的结果[3]。
为了应对来自真实世界的挑战,让更多患者能够通过细胞治疗这一途径解决以往难以治疗的疾病,现存的细胞治疗技术亟需进一步改进和创新升级。更强靶向性、更具安全性、以及通用“现货型”的细胞治疗产品已经在路上,我们期待更多新材料、新技术和创新治疗策略,能够解决更多未满足的临床痛点。复宏汉霖2022火星登陆计划,期待有志之士的加入!
