2026年3月5日,复宏汉霖(2696.HK)宣布,公司自研的口服创新赖氨酸乙酰转移酶6A/B(KAT6A/B)小分子抑制剂HLX97的新药临床试验(IND)申请已获得国家药品监督管理局(NMPA)批准,拟用于晚期或转移性实体瘤的治疗,有望为乳腺癌等实体瘤耐药患者带来新的治疗方案。
潜在同类最优:精准抑制KAT6A/B,挑战后线治疗
KAT6A(Lysine Acetyltransferase 6A)及其旁系同源物KAT6B(Lysine Acetyltransferase 6B)是MYST 家族的组蛋白赖氨酸乙酰转移酶(HAT),在多种肿瘤的发生发展和耐药性产生中发挥着关键作用。临床前及临床研究显示,在既往接受过多种治疗的ER+/HER2-转移性乳腺癌患者中,KAT6A基因的扩增/过表达与内分泌治疗耐药性的产生密切相关。此外,也观察到 KAT6A/B基因的异常表达出现在卵巢癌、子宫颈癌、结直肠癌、前列腺癌、肺癌和脑胶质瘤中等多种实体瘤中1-3,提示KAT6A/B抑制剂在多类肿瘤的治疗中具有潜在的应用前景。
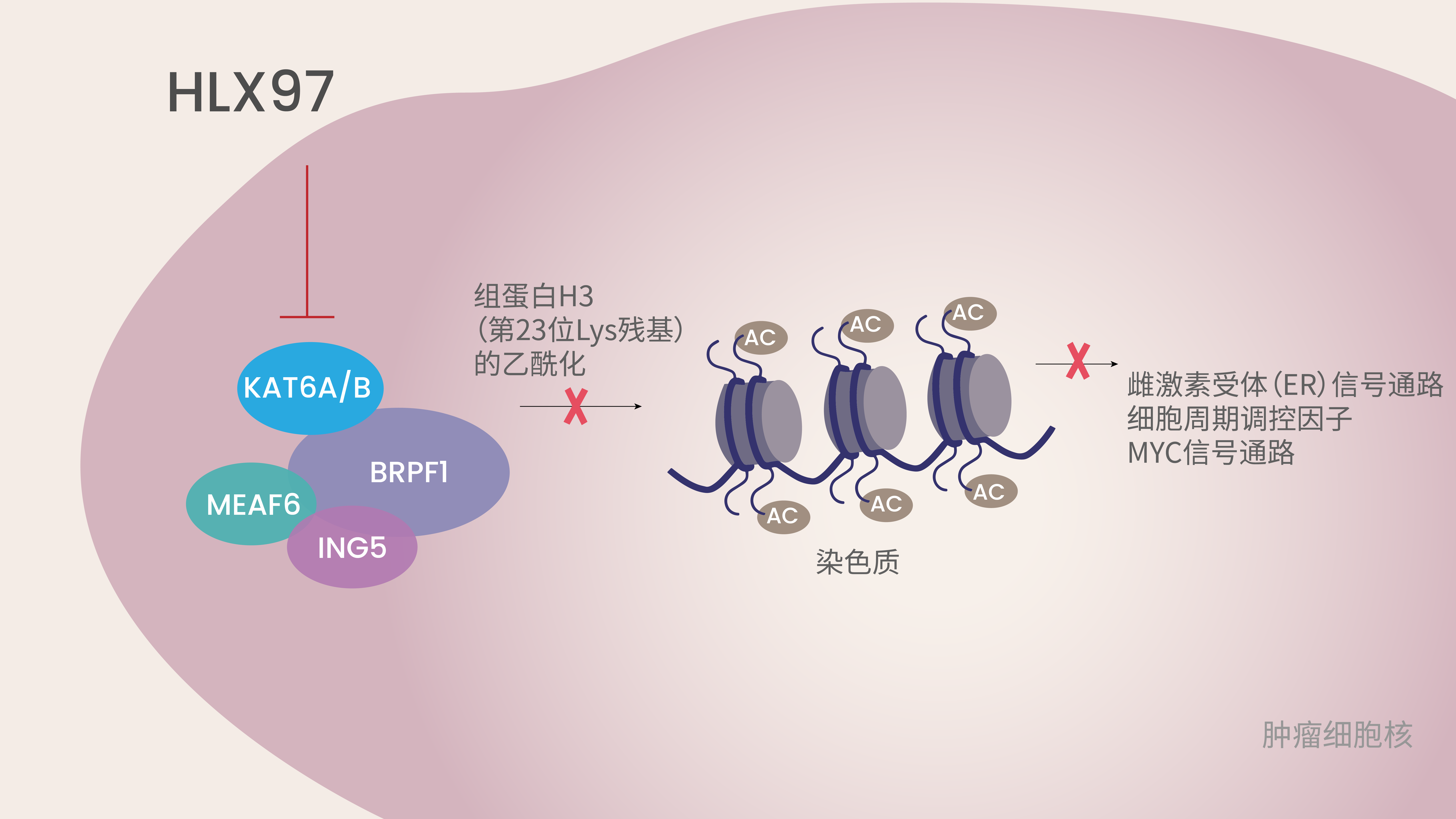
HLX97 是一款具有同类最优潜力的创新型口服KAT6A/B抑制剂。通过精准抑制KAT6A/B的活性,HLX97能够调控肿瘤细胞的增殖,诱导肿瘤细胞凋亡,具有“快速起效、快速清除”药代动力学特性和高选择性,旨在最大化药物抗肿瘤活性的同时减轻产品的血液毒性。非临床研究显示,HLX97具有良好的抗肿瘤效果和安全性。与同类产品PF-07248144相比,HLX97展现出更强的KAT6A/B抑制活性和对KAT5/7/8更高的选择性,其中,HLX97在更低剂量下即展现出与同类产品相当或更优的抗肿瘤活性;在相近抑瘤水平时,HLX97引发的血液学毒性显著更低,预示其在临床上可能拥有更宽的治疗窗口。同时,HLX97显示出良好的ADME特性,包括高口服生物利用度和优异的药代动力学特征4-5。
全域全程全球:构建乳腺癌全生命周期治疗生态
乳腺癌是全球第二以及女性最高发的恶性肿瘤,成为导致女性癌症死亡的主要原因。其中,ER+乳腺癌是最常见的乳腺癌亚型,约占所有乳腺癌病例的70%6。尽管抑制雌激素生成、直接靶向ER的干预措施等内分泌治疗已成为其基石疗法,显著降低了ER+乳腺癌的复发率和死亡率,但新生耐药和获得性耐药仍然是一项重大挑战。鉴于乳腺癌中KAT6A基因的扩增/过表达已被证实与内分泌治疗耐药性的产生密切相关。因此,靶向抑制KAT6A/B活性有望成为一种克服耐药的有效策略7-9。
HLX97成功获批临床,标志着复宏汉霖已经构建了完整贯通的小分子药物研发能力。从成熟靶点的差异化开发到新兴靶点的战略布局,公司正加速实现大分子与小分子药物的深度融合与优势互补。通过自主研发与战略引进,复宏汉霖已在乳腺癌领域建立了“全域全程全球”的完整治疗生态,产品管线包括中美欧等全球50多个国家和地区获批上市曲妥珠单抗生物类似药汉曲优®(美国商品名:HERCESSI™,欧洲商品名:Zercepac®),首个美国获批的帕妥珠单抗生物类似药POHERDY®,早期强化辅助治疗药物汉奈佳®(奈拉替尼),创新CDK4/6抑制剂复妥宁®(伏维西利)等上市产品,以及新表位抗HER2单抗HLX22、新型内分泌疗法拉索昔芬片HLX78、LIV-1靶点ADC HLX41、HER2xHER2双表位ADC HLX49、HER2 ADC HLX87等高潜创新分子,持续推进覆盖乳腺癌各分型分期的单药及联合疗法临床研究,通过强化管线协同效应,持续提升覆盖提升治疗价值。
未来,复宏汉霖将继续坚持“以患者为中心”的研发理念,依托平台化、系统化的创新体系,加速推进具有全球竞争力的差异化创新管线布局,为全球患者提供更可及、更有效的治疗选择。
【参考文献】
1. Chen J, et al. Mutations of Chromatin Structure Regulating Genes in Human Malignancies. Curr Protein Pept. Sci. 2016;17(5):411-437.
2. Partynska A, et al. The Expression of Histone Acetyltransferase KAT6A in Non-small Cell Lung Cancer. Anticancer Res. 2022;42(12):5731-5741.
3. Lv D, et al. Histone Acetyltransferase KAT6A Upregulates PI3K/AKT Signaling through TRIM24 Binding. Cancer Res. 2017;77(22):6190-6201.
4. Liu R, et al. Abstract 6976: Identification of novel KAT6A/B inhibitors with enhanced antitumor activity and reduced hematologic toxicity. Cancer Res (2025) 85 (8_Supplement_1): 6976. AACR Annual Meeting 2025.
5. 2026年第44届摩根大通医疗健康年会复宏汉霖投资者推介材料
6. Nolan E, et al. Deciphering breast cancer: from biology to the clinic. Cell. 2023;186(8):1708-1728.
7. Sharma S, et al. Discovery of a highly potent, selective, orally bioavailable inhibitor of KAT6A/B histone acetyltransferases with efficacy against KAT6A-high ER+ breast cancer. Cell Chem Biol. 2023;30(10):1191-1210.e20.
8. Yu L, et al. Identification of MYST3 as a novel epigenetic activator of ERα frequently amplified in breast cancer. Oncogene. 2017;36(20):2910-2918.
9. Yu L, et al. Identification of MYST3 as a novel epigenetic activator of ERα frequently amplified in breast cancer. Oncogene. 2017;36(20):2910-2918. doi:10.1038/onc.2016.433

