双重免疫逃逸精准破局
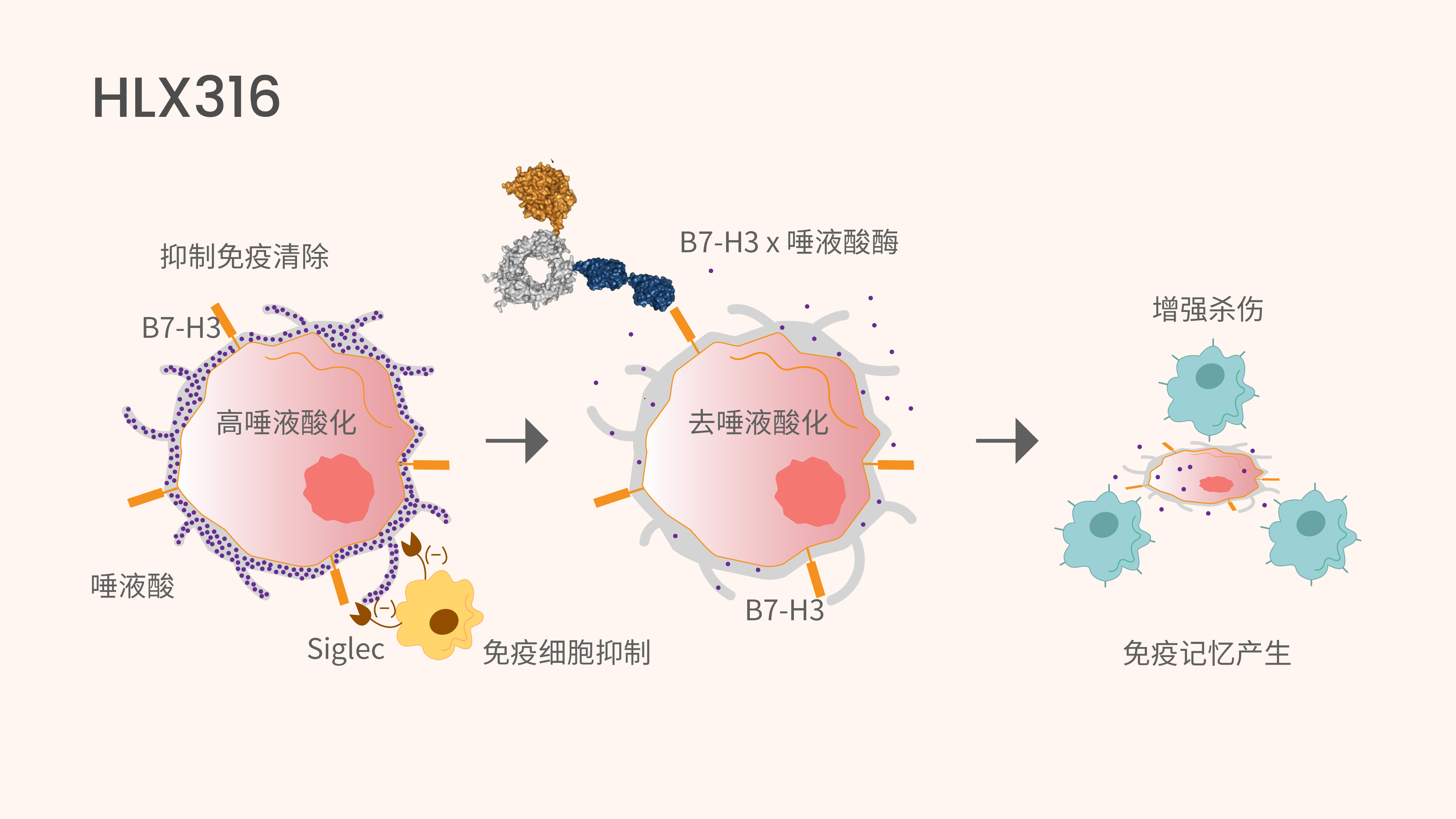
HLX316是一款基于蛋白工程平台开发的靶向B7同源物3(B7-H3/CD276)的人唾液酸酶融合蛋白。HLX316针对癌症中两种关键的免疫逃逸途径,即B7-H3过表达和肿瘤高唾液酸化。B7-H3是一种免疫检查点蛋白,在肺癌、乳腺癌、结直肠癌、胰腺癌、前列腺癌和卵巢癌等多种实体肿瘤中过表达,其与肿瘤进展和预后不良相关,但在正常组织中的表达水平很低。肿瘤高唾液酸化可以衔接白细胞上的抑制性 Siglec 受体,从而削弱先天性和适应性免疫效应功能,导致免疫检查点抑制剂(ICI)耐药性。HLX316通过酶促作用去除末端唾液酸,并浓缩其在B7-H3阳性肿瘤细胞中的活性,从而解除糖免疫检查点抑制,恢复肿瘤微环境内的先天性和适应性免疫介导的抗肿瘤功能。
通过靶向表达B7-H3 的肿瘤细胞及其微环境发挥唾液酸酶活性,HLX316有潜力同时缓解蛋白和聚糖介导的免疫抑制,拓宽免疫治疗在实体瘤中的应用范围,突破现有治疗方案局限。临床前研究显示,HLX316对肿瘤细胞具有强效的B7-H3 定向去唾液酸化作用,且具有良好的耐受性。
体系化创新驱动多元差异管线
HLX316为公司基于与Palleon战略合作开展的创新项目之一。Palleon由联合创始人、诺贝尔奖获得者Carolyn Bertozzi教授共同创立,其在糖生物学领域的突破性发现促成了公司技术平台的开发。双方将依托各自在糖生物学与肿瘤免疫领域的技术积累,加速推进创新融合蛋白药物的全球研发进程。HLX316的IND获批,是公司创新引擎持续加速运转的又一体现。依托PD(L)1为核心的免疫检查点抑制剂平台、免疫细胞衔接器平台(如多特异性TCE平台)、Hanjugator™ ADC平台、免疫细胞衔接器及AI驱动的一站式早期研发平台HAI Club,公司正系统性构建覆盖多抗、ADC、融合蛋白及小分子抑制剂在内的多技术路径创新体系。
在这一创新框架下,多款差异化分子已进入密集推进阶段。HLX37(PD-L1×VEGF双特异性抗体)IND获批并完成首例患者给药;HLX701(SIRPα-Fc融合蛋白)已启动II期临床研究;基于自研T细胞衔接器(TCE)平台开发的DLL3xDLL3xCD3xCD28四特异性TCE HLX3901、HLX97(KAT6A/B抑制剂)与HLX316同步获得IND受理。与此同时,HLX3902(STEAP1×CD3×CD28三特异性TCE)、HLX49(HER2×HER2 ADC)、HLX48(EGFR×cMET ADC)、HLX105(抗体融合蛋白)在内的多个前沿项目也正加速向临床转化,形成梯度清晰、技术多元的早期产品矩阵。
复宏汉霖正在打造具备持续输出能力的创新管线体系。随着核心产品进入全球关键性临床阶段,并逐步迈向注册与商业化,复宏汉霖已从“创新突破”迈入“体系化创新”的新阶段。展望未来,公司将持续深化全球化2.0战略布局,在保持稳健现金流支撑研发投入的同时,加速差异化创新资产的全球开发与转化,推动更多具有国际竞争力的产品走向欧美成熟市场,朝着2030年“迈向全球的生物制药企业”的愿景稳步前行。
