2026年美国临床肿瘤学会(ASCO)年会将于5月29日-6月2日在美国芝加哥隆重召开。本届学术会议上,复宏汉霖将重磅发布公司创新管线中十余项研究的进展,覆盖抗PD-1单抗H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)、HLX43(PD-L1 ADC)、抗EGFR单抗pimurutamab(HLX07)和创新CDK4/6抑制剂复妥宁®(枸橼酸伏维西利胶囊)等创新分子的最新/更新研究数据,聚焦肺癌、乳腺癌和消化道肿瘤等领域,多个潜在“同类首创(FIC)”领域布局加速进入临床验证阶段。
其中,两项研究成功入选口头报告,包括由北京大学肿瘤医院季加孚、沈琳教授牵头的H药胃癌围术期III期研究(ASTRUM-006),以及由中国医学科学院肿瘤医院王洁教授牵头的HLX43在非小细胞肺癌中的研究,凸显公司核心创新资产在全球顶尖学术舞台的持续突破。此外,复妥宁®注册性研究结果也将首次发布。
H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)
H药是全球首个获批一线治疗小细胞肺癌(SCLC)的抗PD-1单抗,目前已在中国、英国、欧盟、新加坡、印度、瑞士、秘鲁等40多个国家和地区获批上市。2022年3月,H药正式在中国获批上市,目前可用于治疗鳞状非小细胞肺癌(sqNSCLC)、广泛期小细胞肺癌(ES-SCLC)、食管鳞状细胞癌(ESCC)及非鳞状非小细胞肺癌(nsqNSCLC)。
H药持续在肺癌和消化道肿瘤上取得突破,剑指多项“全球首个”。继成为全球首个获批一线治疗SCLC的抗PD-1单抗,H药也是全球首个胃癌围术期以免疫单药取代术后辅助化疗的治疗方案。在中国,H药获得国家药品监督管理局突破性疗法认定用于胃癌围手术期治疗,相关上市申请已获受理并纳入优先审评,并有望于2026年获批。在欧盟,H药治疗nsqNSCLC和ESCC的适应症也已于2026年获得上市申请积极意见。在美国,H药一线治疗ES-SCLC的美国桥接试验已完成患者入组,计划2026年向FDA递交相应生物制品许可申请(BLA)。随着全球商业化势能与差异化临床价值的加速释放,H药目标成为下一款全球年销售额突破百亿人民币的国产创新药。

HLX43(PD-L1 ADC)
HLX43是一款靶向程序性死亡-配体1(PD-L1)的新型ADC候选药物,由全人源IgG1抗PD-L1抗体与创新连接子-拓扑异构酶抑制剂荷载偶联而成,其药物抗体比(drug-to-antibody ratio, DAR)约为8。HLX43兼具毒素精准杀伤和肿瘤免疫作用的复合功能,其毒素不仅能够藉靶点内吞进入肿瘤细胞后进行释放,并在肿瘤微环境中释放后借助旁观者效应进入肿瘤细胞,阻断DNA复制,从而导致肿瘤细胞凋亡。此外,HLX43的PD-L1靶向抗体可激活免疫调节机制,发挥协同抗肿瘤效应。
HLX43首次人体研究结果、多项实体瘤概念验证数据先后亮相多场国际学术大会,展现出“高效、低毒”的显著疗效,尤其在NSCLC人群中不依赖生物标志物筛选,有望覆盖所有亚型患者。除NSCLC外,HLX43已在妇科肿瘤、食管鳞癌等多个实体瘤中展现积极疗效信号。单药之外,公司也积极探索其与抗EGFR单抗pimurutamab、H药等药物的联合治疗潜力。

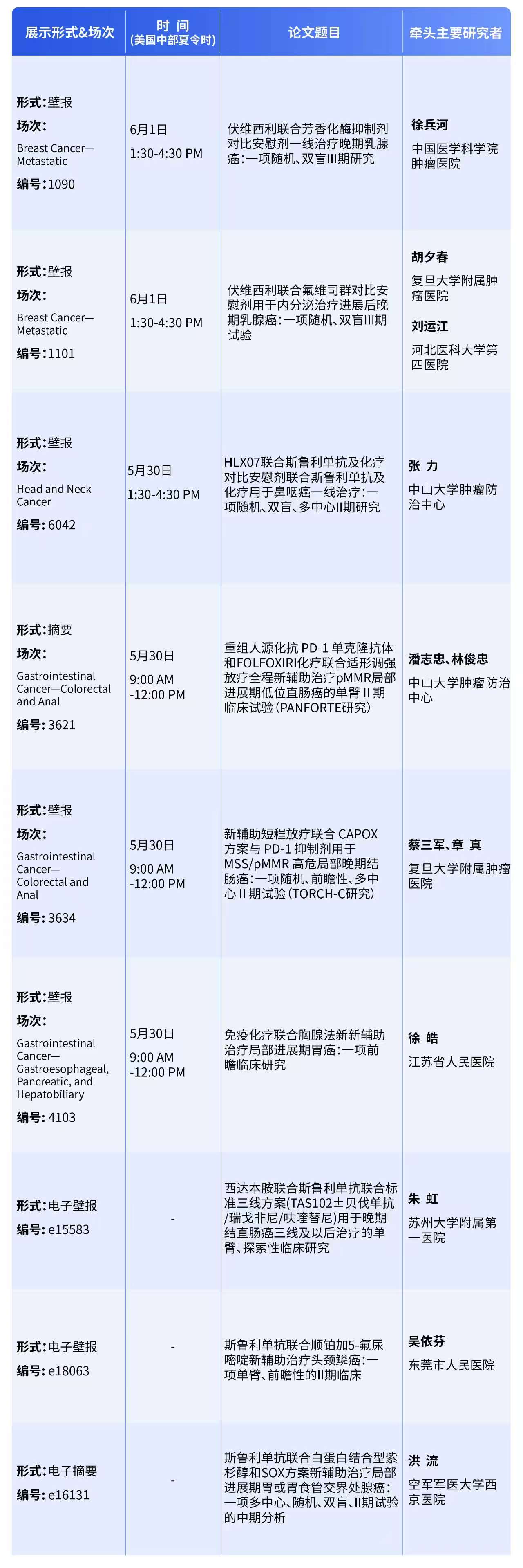
此外,复宏汉霖还将在本届ASCO大会上展示多项创新管线的最新进展,包括已获批上市的创新CDK4/6抑制剂复妥宁®(枸橼酸伏维西利胶囊)和抗EGFR单抗pimurutamab等在研产品,以及围绕H药开展的一系列研究者发起研究(IIT)。相关研究的摘要信息如下: