2022年11月5日至11月12日,第25屆全國臨床腫瘤學大會暨2022年CSCO學術年會以線上與線下結合的方式召開。11月5日,復宏漢霖創新抗PD-1單抗H藥 漢斯狀®(斯魯利單抗)在食管鱗狀細胞癌(ESCC)中開展的關鍵性III期臨床研究數據已於全體大會首次發佈並獲選優秀論文,該研究由中國醫學科學院腫瘤醫院黃鏡教授進行了口頭報告,同步也將於11月12日在食管癌專場由中國醫學科學院腫瘤醫院宋岩教授進行口頭報告。
以下為H藥針對食管鱗癌III期臨床研究的數據詳情:
論文題目:First-line serplulimab versus placebo in combination with chemotherapy in PD-L1-positive esophageal squamous cell carcinoma (ASTRUM-007): a randomized, double-blind, multicenter phase 3 study
聯合主要研究者:黃鏡 國家癌症中心/國家腫瘤臨床醫學研究中心/中國醫學科學院北京協和醫學院腫瘤醫院
展示形式:口頭報告
主講人:黃鏡 國家癌症中心/國家腫瘤臨床醫學研究中心/中國醫學科學院北京協和醫學院腫瘤醫院
匯報地點:北京會場,全體大會
匯報時間:11月5日 11:05-11:20
論文題目:First-line serplulimab versus placebo in combination with chemotherapy in PD-L1-positive esophageal squamous cell carcinoma (ASTRUM-007): a randomized, double-blind, multicenter phase 3 study
聯合主要研究者:黃鏡 國家癌症中心/國家腫瘤臨床醫學研究中心/中國醫學科學院北京協和醫學院腫瘤醫院
展示形式:口頭報告
主講人:宋岩 國家癌症中心/國家腫瘤臨床醫學研究中心/中國醫學科學院北京協和醫學院腫瘤醫院
匯報地點:廣州會場,食管癌專場
匯報時間:11月12日 15:30-15:40
試驗設計
本隨機、雙盲、III期臨床試驗在中國70家醫院展開。腫瘤標本PD-L1陽性(CPS ≥1)、既往未接受過治療的局部晚期或轉移性食管鱗癌(ESCC)患者按照2:1比例隨機入組,分別每兩周一次接受3 mg/kg斯魯利單抗或安慰劑(最多兩年)聯合化療(50 mg/m2順鉑 + 每周期第1-2天每天1200 mg/m2 5-氟尿嘧啶)。研究的共同主要終點為全人群中盲態獨立評審委員會評估的無進展生存期(PFS)和總生存期(OS)。次要終點包括客觀緩解率(ORR)、緩解持續時間(DOR)、安全性、藥代動力學特徵和免疫原性。

試驗結果
在2019年6月19日至2021年12月17日期間,共入組並隨機分配551名患者進入斯魯利單抗聯合化療組(n=368)和安慰劑聯合化療組(n=183)。中位隨訪時間為14.9個月。斯魯利單抗聯合化療組中的中位PFS(最終分析)相對於安慰劑聯合化療組的中位PFS有顯著延長【5.8個月(95% CI 5.7–6.9)和5.3個月(95% CI 4.3–5.6),風險比(HR)為0.60(95% CI 0.48–0.75;p<0.001)】。斯魯利單抗聯合化療組中的中位OS(期中分析)相對於安慰劑聯合化療組的中位OS也獲得了顯著改善【15.3個月(95% CI 14.0–18.6)和11.8個月(95% CI 9.7–14.0),HR為0.68(95% CI 0.53–0.87;p=0.0020)】。
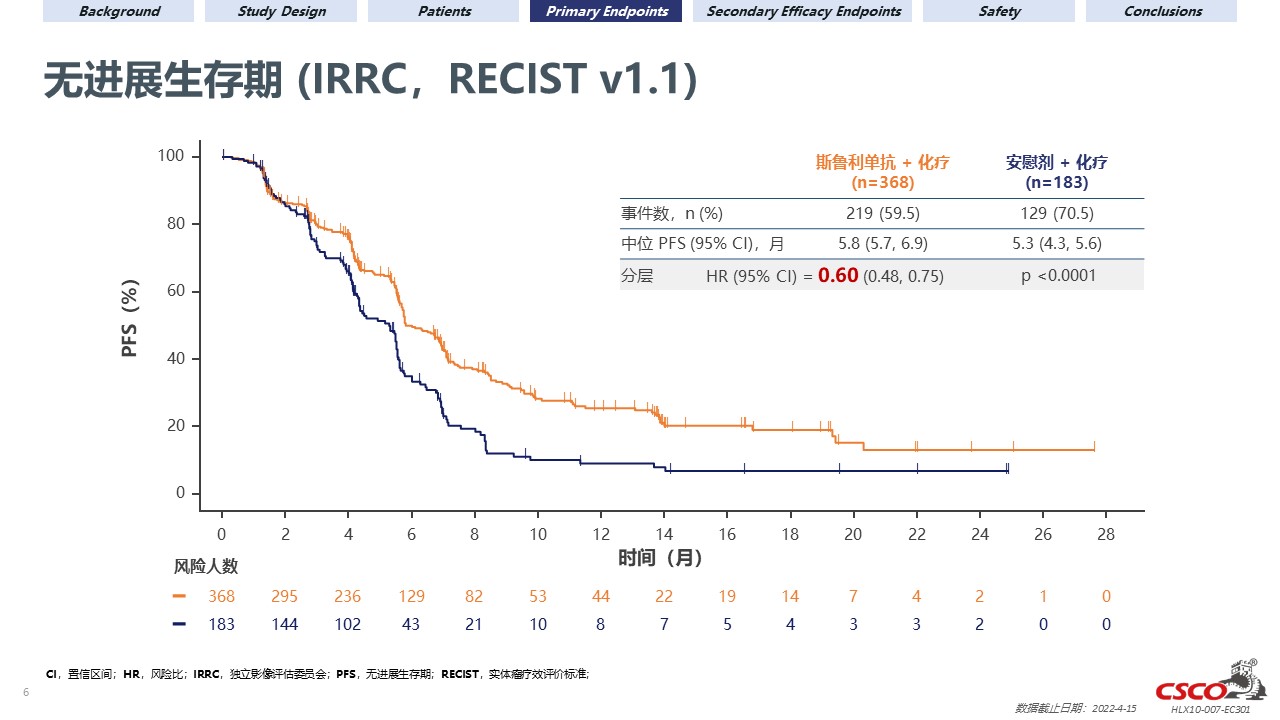
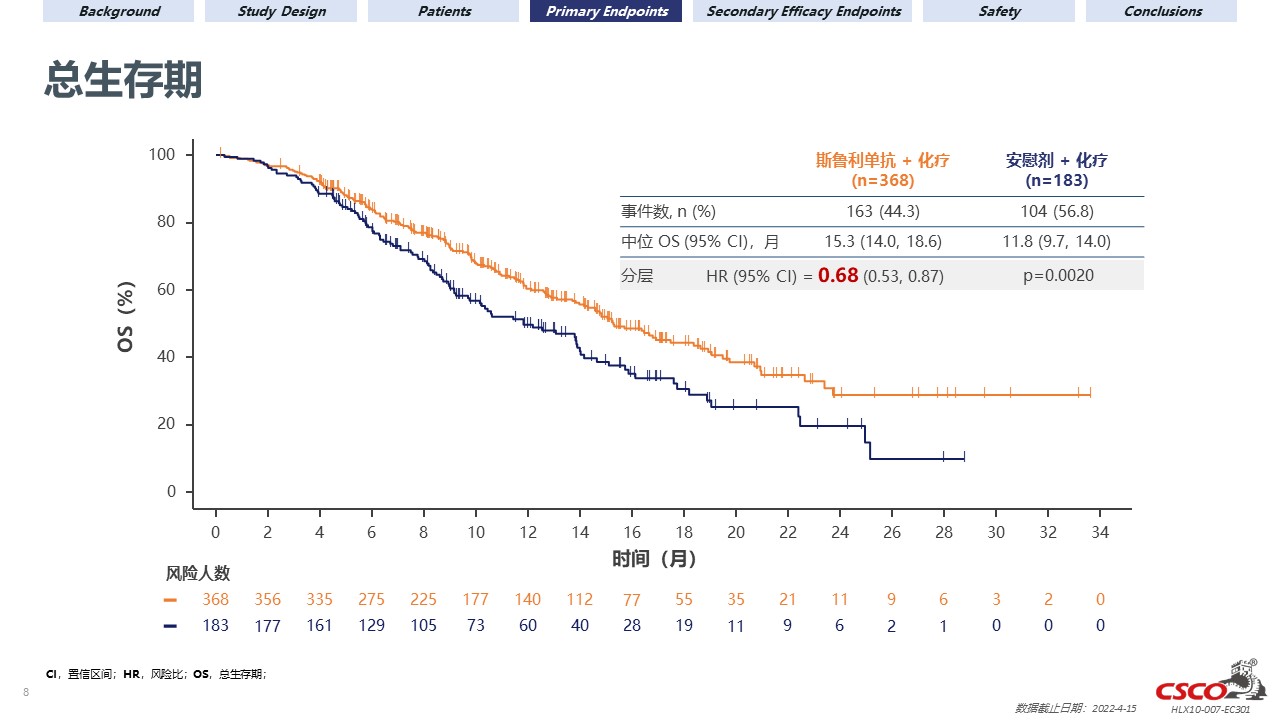
由盲態獨立評審委員會評估的兩組的ORR分別為57.6%(95% CI 52.4–62.7;50例完全緩解)和42.1%(95% CI 34.8–49.6;12例完全緩解)。
斯魯利單抗聯合化療組和安慰劑聯合化療組分別有201(52.6%)及81(48.2%)名患者發生三級及以上與治療相關的不良事件(TRAEs)。兩組分別有11(2.9%)和3(1.8%)名患者發生了與治療相關的死亡。斯魯利單抗組的三級及以上免疫相關不良事件(irAEs)發生率較安慰劑組高(8.6% 和2.4%),且與已獲批的PD-1/PD-L1單抗相似。
結論
試驗結果表明,斯魯利單抗聯合化療每兩周一次給藥能明顯改善一線、PD-L1陽性、晚期ESCC患者的PFS和OS,且其安全性良好。斯魯利單抗聯合化療有望為此類患者提供一種新的治療選擇。
