近日,復宏漢霖(2696.HK)於ADC Asia Congress 2026上首次披露其自主研發的靶向CDH17的抗體藥物偶聯物(ADC)HLX403的臨床前研究數據。這款基於復宏漢霖自主知識產權Hanjugator™ ADC平台開發的候選分子展現出多維度的差異化優勢,有望為消化道腫瘤的治療提供一款更優的ADC候選分子。
消化道腫瘤(gastrointestinal cancers,GI cancers)是全球範圍內疾病負擔最重的癌症之一,每年新發病例超過500萬,死亡病例約370萬1,其中結直腸癌與胃癌長期位居發病率和死亡率前列,胰腺癌則以侵襲性強、預後差為特徵,被視為致死率最高的實體瘤之一。儘管靶向治療和免疫治療的快速發展改善了部分患者的治療結局,但相當比例的消化道腫瘤患者尤其是晚期或轉移性患者,仍面臨治療選擇有限、療效持續性不足以及獲得性耐藥等挑戰,提示該疾病領域仍存在顯著的未滿足臨床需求2。近年來,抗體藥物偶聯物(ADC)憑藉其精準的腫瘤殺傷機制,已成為消化道腫瘤領域的前沿研究方向及臨床開發熱點,靶向HER2、Claudin18.2、CDH17、c-MET等ADC藥物研發進展迅速,顯示出良好的抗腫瘤活性及可管理的安全性特徵,有望進一步拓展消化道腫瘤患者的精準治療策略3。

其中,Cadherin-17(CDH17)屬於鈣黏蛋白家族,通常在胃腸上皮細胞的緊密連接處表達。在胃癌、結直腸癌和胰腺癌等多類消化道腫瘤中,CDH17呈現高表達,且表達水平與患者的不良預後密切相關。由於CDH17在正常組織中表達受限,而在惡性腫瘤細胞表面暴露,這一選擇性表達特徵使其成為開發更精準ADC療法的重要靶點4-5。
此次公佈的多項臨床前研究結果顯示該分子具備:
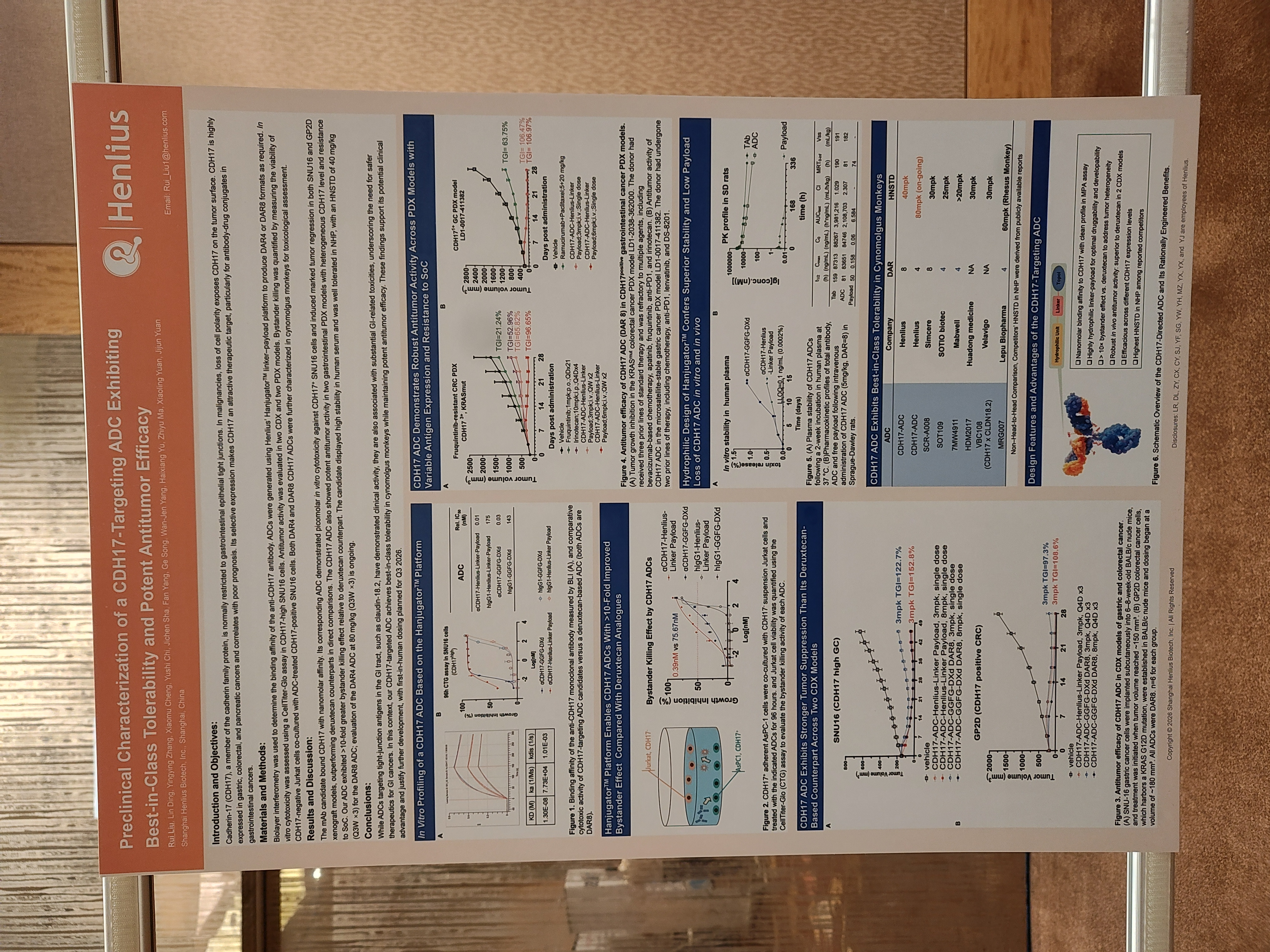
1. 卓越的抗體性能與特異性
• 高親和力與特異性: 該ADC使用的抗體對CDH17具有納摩爾級(nanomolar)的結合親和力;不會與鈣粘蛋白家族的其他成員發生脫靶結合,且在MPA檢測中表現乾淨。
2. 立足差異化的連接子-載荷(Linker-Payload)平台(HanjugatorTM)
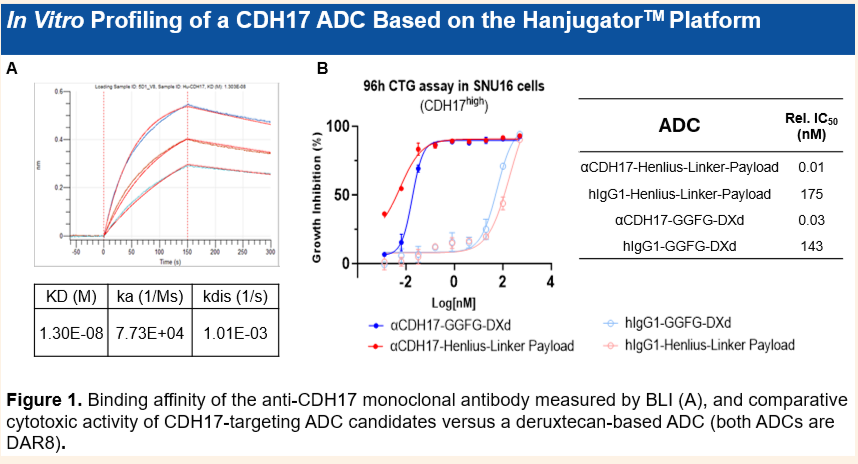
• 高親水性設計: 採用自主研發的親水性Linker-Payload平台,具有極佳的成藥性和可開發性。
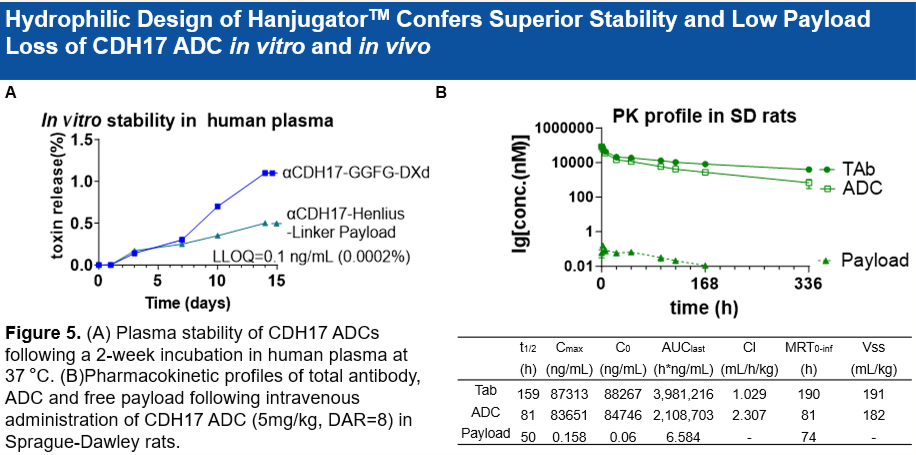
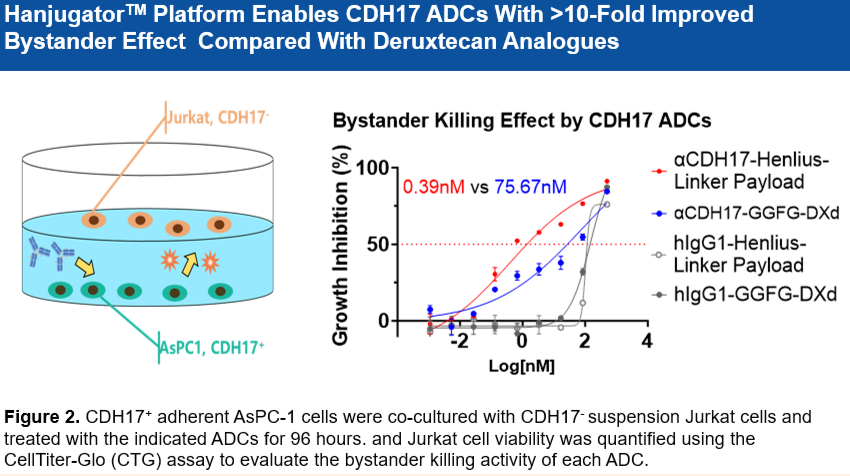
• 載荷(Payload)的活性與DXd相當,且具有強大的旁觀者殺傷效應(Bystander Effect):該ADC的旁殺傷效應是基於deruxtecan ADC的19.7倍,有助於解決腫瘤的異質性問題。
3. 強效的體內抗腫瘤活性&耐藥性腫瘤治療潛力
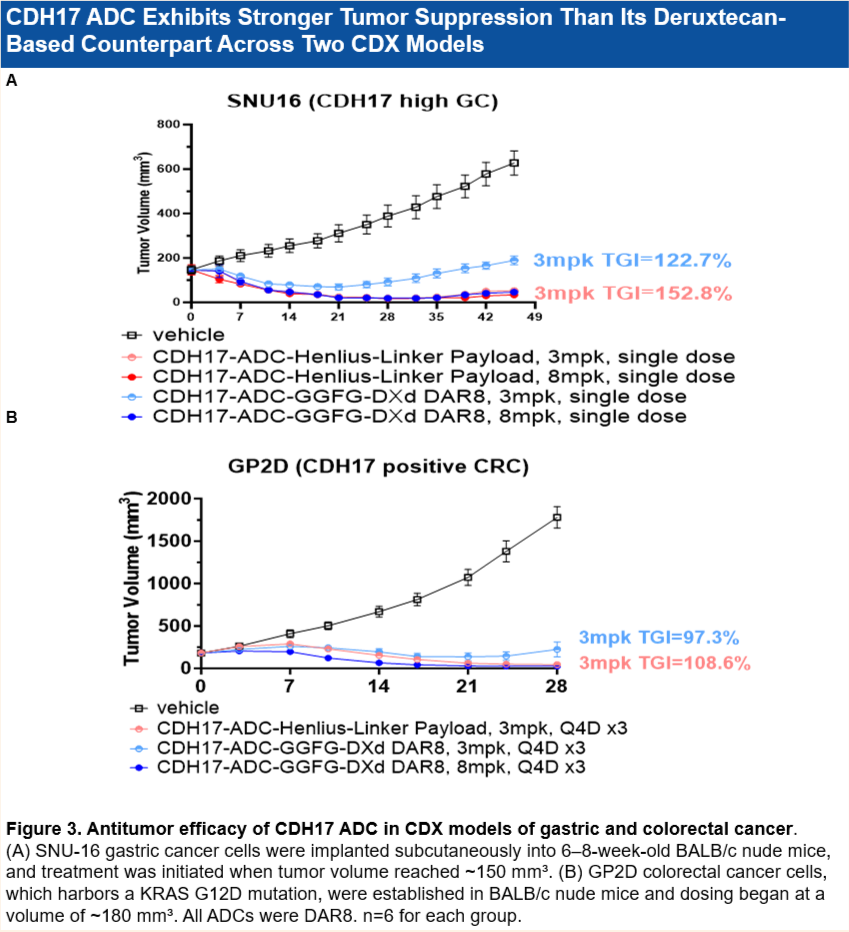
• 優於deruxtecan: 在多個CDX模型(如SNU16胃癌和GP2D結直腸癌)中,其療效優於deruxtecan。
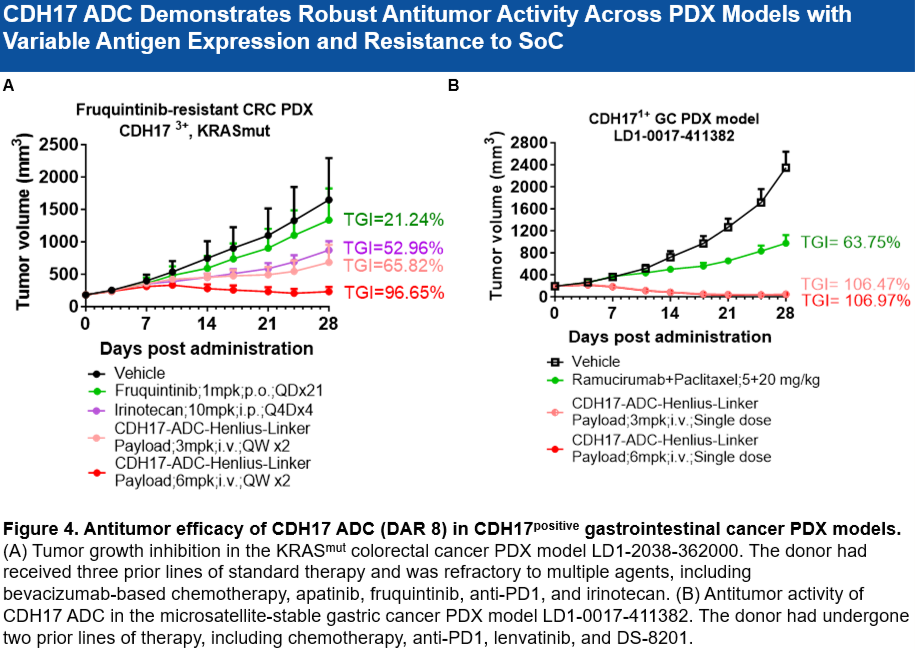
• 克服耐藥性: 在對呋喹替尼(Fruquintinib)耐藥的KRAS突變結直腸癌(CRC)PDX模型中顯示出強勁療效。
• 對低表達腫瘤有效: 在CDH17低表達、PD-L1低表達的胃癌(GC)PDX模型中,單次給藥(3 mpk或 6 mpk)即可達到超100%的腫瘤生長抑制率(TGI)。
4. 潛在最優的安全性與耐受性
• 同類最優的安全性: 在非人靈長類動物(NHP)的毒理研究中,其最高非嚴重毒性劑量(HNSTD)達到40 mpk(Q3W x 3),在所有已知的同靶點ADC中處於最高水平。
• 良好的CMC特性: 抗體滴度高(>8 g/L),整體CMC屬性良好。
綜上所述,復宏漢霖的CDH17 ADC HLX403在臨床前研究中展現了強效的抗腫瘤活性,同時在非靈長類動物中顯示出同類最優的耐受性,有望突破腫瘤異質性和耐藥性腫瘤的治療瓶頸,為消化道腫瘤患者帶來潛在更優的ADC治療選擇。該分子有望於2026年啟動首次人體臨床試驗。
【參考文獻】
1.Danpanichkul P, et al. Epidemiology of gastrointestinal cancers: a systematic analysis from the Global Burden of Disease Study 2021. Gut. 2024 Dec 10;74(1):26-34.
2.Singh A. Global burden of five major types of gastrointestinal cancer. Prz Gastroenterol. 2024;19(3):236-254.
3.Ntellas P, Chau I. Expanding the potential of antibody-drug conjugates in gastrointestinal malignancies: beyond HER2 targets. ESMO Gastrointest Oncol. 2025;8:100154.
4.Ge J, et al. A clinicopathological study on the expression of cadherin-17 and caudal-related homeobox transcription factor (CDX2) in human gastric carcinoma. Clin Oncol (R Coll Radiol). 2008 May;20(4):275-83.
5.Ito R, et al. Clinicopathological significant and prognostic influence of cadherin-17 expression in gastric cancer. Virchows Arch. 2005 Oct;447(4):717-22.
